DERS 2
ÜNİTE 3: MADDENİN TANECİKLİ YAPISI
KONU: ELEMENTLER-BİLEŞİKLER-MOLEKÜLLER
KARIŞIMLAR
MADDELERİN SINIFLANDIRILMASI
Maddeler saf ve saf olmayan maddeler şeklinde iki ana grupta toplanır.
1-Saf madde: Her yerinde aynı özelliğe sahip olan maddelere saf madde denir.
Element ve bileşikler saf maddedir, karışımlar ise saf madde değildir.
Saf maddelerin öz kütle, çözünürlük, öz ısı, erime noktası ve kaynama noktası gibi ayırt edici özellikleri vardır.
Saf maddelere örnekler: Bakır, hidrojen, demir, oksijen, helyum v.b (elementlerin hepsi)
Saf su, karbondioksit, tuz, şeker, amonyak v.b (bileşiklerin hepsi)
.jpg)
Element ve bileşikler saf maddelerdir.
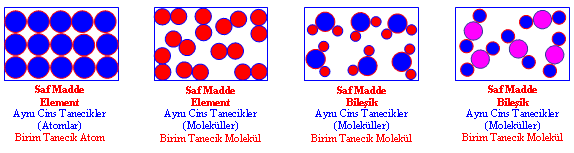
Element: Aynı cins atomlardan meydana gelen saf maddeye element denir.
.jpg)
2-Saf olmayan maddeler (Karışımlar):

Özellikleri her yerinde aynı olmayan ve dışarıdan bakıldığında tek bir madde gibi gözükmeyen karışımlara heterojen karışım denir.
.jpg) |
| Element atomları Element molekülü Karışımlar |
 |
| Çeşme suyu içinde mineraller olduğu için saf değildir. |
Element ve bileşikler saf maddedir, karışımlar ise saf madde değildir.
Saf maddeler aynı cins atom yada moleküllerden meydana gelir.
Aynı cins atomlardan oluşanlara element, iki ya da daha fazla farklı cins atomdan
oluşanlara ise bileşik denir. Bileşikler aynı cins moleküllerden oluşmuştur.
Saf maddelerin öz kütle, çözünürlük, öz ısı, erime noktası ve kaynama noktası gibi ayırt edici özellikleri vardır.
Saf maddelere örnekler: Bakır, hidrojen, demir, oksijen, helyum v.b (elementlerin hepsi)
Saf su, karbondioksit, tuz, şeker, amonyak v.b (bileşiklerin hepsi)
.jpg)
Element ve bileşikler saf maddelerdir.
Element: Aynı cins atomlardan meydana gelen saf maddeye element denir.
Demir, bakır, oksijen,klor,helyum,kurşun,gümüş,altın element örnekleridir.
Elementler sembollerle gösterilir.
Elementler fiziksel veya kimyasal yollarla daha basit maddelere ayrılmaz.
Elementler Neden Sembollerle Gösterilir?
Kimyasal işlemlerde maddelerin Lâtince (bilim dili) isimleriyle işlem yapmak zordur. Bunun yerine elementlerin Lâtince isimlerinin kısaltmalarından oluşan semboller kullanılır.Element sembollerinin uluslararası geçerliliği vardır.
Element sembollerinde ilk harf her zaman büyük, varsa diğerleri daima küçük yazılır.
Örnekler:
Hidrojen H Helyum He Karbon C Demir Fe
Kalsiyum Ca Bor B Berilyum Be Sodyum Na
 |
| Element Element Molekülleri Bileşik Molekülleri |
Molekül
Maddenin tüm özelliğini taşıyan en küçük birimine molekül denir.
Moleküller maddenin tüm özelliklerini gösterir ve bağımsız olarak hareket edebilir.
Örnek: H2O, CO2,H2, O2 molekülü.
Aynı cins atomlardan oluşan moleküllere element molekülleri denir.
Aynı cins atomlardan oluşan moleküllere element molekülleri denir.
Cl2,O2, H2, F2, N2 , I2 element molekülleridir. Bunlar bileşik değildir.
Bileşikler: İki ya da daha fazla cins atomdan meydana gelen saf maddeye bileşik denir.
Su, karbondioksit, amonyak, glikoz, sofra tuzu bileşik örnekleridir.
Bileşikler formüllerle gösterilir.
Elementlerin belirli oranlarda birleşmesiyle meydana gelir.
Kendisini oluşturan elementlerin özelliklerinden tamamen farklı özellik taşır.
Kendilerini oluşturan elementlere kimyasal yollarla ayrıştırılabilir.
Bileşikler formüllerle gösterilir.
Elementlerin belirli oranlarda birleşmesiyle meydana gelir.
Kendisini oluşturan elementlerin özelliklerinden tamamen farklı özellik taşır.
Kendilerini oluşturan elementlere kimyasal yollarla ayrıştırılabilir.
 |
| Glikoz Molekülü |
Farklı cins atomların molekülleri bileşik moleküllerini oluşturur.
H2O, CO2, C6H12O6 , NH3 bileşik molekülleridir.
.jpg)
2-Saf olmayan maddeler (Karışımlar):
Birden fazla maddenin rasgele miktarlarda bir araya gelmesiyle oluşan madde topluluğuna karışım denir.
Şekerli su, tuzlu su, salata, çorba, petrol, hava, kağıt gibi maddeler birer karışımdır.
Şekerli su, tuzlu su, salata, çorba, petrol, hava, kağıt gibi maddeler birer karışımdır.
Karışımların hazırlanmasında belirli bir oran yoktur.
Karışımlar, maddelerin birbiri içindeki dağılımına göre homojen ve heterojen olarak iki grupta incelenir.
a)Homojen Karışımlar (Çözeltiler):
Karışımlar, maddelerin birbiri içindeki dağılımına göre homojen ve heterojen olarak iki grupta incelenir.
a)Homojen Karışımlar (Çözeltiler):
Özellikleri her yerinde aynı olan ve dışarıdan bakıldığında tek bir madde gibi gözüken karışımlara homojen karışımlar denir.
Çözünen + Çözücü = Çözelti ( Homojen Karışım )
Çözelti: Bir maddenin diğer bir madde içerisinde her tarafa eşit olarak dağılmasıyla oluşan karışımlara denir. Çözeltiler homojen karışımlardır.
Tuzlu su, şekerli su, hava, maden suyu, alkollü su, gazoz, alaşımlar, kolonya….
Bütün gaz karışımları çözeltidir.
Çözünme: Bir maddenin diğer bir madde içerisinde gözle görülmeyecek şekilde dağılmasına çözünme denir.
Çözünme hızını etkileyen faktörler: Maddeyi ufalamak, çözeltiyi karıştırmak,çözeltiyi çalkalamak, çözeltinin sıcaklığını arttırmak
b)Heterojen karışımlar( Adi karışımlar)
b)Heterojen karışımlar( Adi karışımlar)

Özellikleri her yerinde aynı olmayan ve dışarıdan bakıldığında tek bir madde gibi gözükmeyen karışımlara heterojen karışım denir.
Ayran, yağlı su, talaş-su karışımı gibi…
Element, Bileşik ve Karışımın Özellikleri
ELEMENT
|
BİLEŞİK
|
KARIŞIM
| |
1
|
Saftır.
|
Saftır.
|
Saf değildir.
|
2
|
Erime noktası sabittir.
|
Erime noktası sabittir.
|
Erime noktası sabit değildir.
|
3
|
Kaynama noktası sabittir.
|
Kaynama noktası sabittir.
|
Kaynama noktası sabit değildir.
|
4
|
Öz kütlesi sabittir.
|
Öz kütlesi sabittir.
|
Öz kütlesi sabit değildir.
|
5
|
Daima homojendir.
|
Daima homojendir.
|
Sadece çözeltiler homojendir.
|
6
|
Daha basit maddelere ayrışmaz.
|
Kimyasal yollarla ayrışır.
|
Fiziksel yollarla ayrışır.
|
7
|
Bileşeni yoktur.
|
Bileşenlerinin özelliklerini taşımaz.
|
Bileşenlerinin özelliklerini taşır.
|
8
|
Yapı taşları atomdur.
|
Yapı taşları moleküldür.
|
Yapı taşları olmaz.
|
.jpg)


.jpg)
4 yorum:
çok güzel ve anlaşılır bir şekilde
çok güzel
çok iyi ve anlaşılıyor
Çok iyi yaaa...
Yorum Gönder